衰老是人们始终不愿意面对的,总是想减缓衰老或者长生不老,最新研究表明,基因突变可能是导致衰老的重要原因。但长久以来,大部分基因突变研究仅局限于人类及其衍生细胞系,对于其他物种的基因突变研究较为匮乏,而关于跨物种体细胞突变率的进化及其在癌症和衰老中的作用的研究更是少之又少。

长期以来,科学家们一直被一个问题所困扰——皮托悖论,因为癌细胞是由单个体细胞基因突变发展而来,那么理论上体型更大、寿命更长的动物应该出现和积累更多基因突变,他们应该更容易发生癌症才对,但实际情况却并非如此。
动物的寿命、体细胞基因突变、癌症发生率、体型大小之间究竟存在着什么关联?为什么不同动物的寿命存在着如此巨大的差异?这些差异与基因突变有关吗?
近期,英国Wellcome Sanger研究所的研究人员在 Nature 上发表题为:Somatic mutation rates scale with lifespan across mammals 的研究论文。该论文还被选为当期封面论文。
这项研究通过对16种不同哺乳动物的全基因组测序结果证实,物种的寿命越长,基因突变发生的速度就越慢。换句话说,尽管在寿命和体型上存在巨大差异,但不同的动物物种往往因为相似数量的基因突变而迎来生命的终结。这为体细胞突变在衰老中发挥长期作用提供了理论支持。


在生物的整个生命周期中,体细胞突变(somatic mutations)发生在所有细胞中。这是一个自然过程,人体细胞每年大约会发生20到50个突变。这些突变大部分是无害的,但其中一些可能会使细胞癌变,走向癌症,或损害细胞的正常功能。
长期以来,科学家们一直猜测体细胞突变的积累会导致衰老,但遗憾的是,由于难以检测单细胞或组织中存在的基因突变,直接研究正常组织中的体细胞突变是十分困难的。所幸,在过去的几年里,随着技术的发展,如在体外将单细胞扩增成克隆群,再进行组织学单位的显微解剖以及单细胞测序或单分子测序,使得在正常组织中的体细胞突变研究成为可能。
在这项最新研究中,研究团队通过全基因组测序技术测量16种哺乳动物的体细胞突变,涵盖了广泛的不同寿命和体重的动物,包括人类、大鼠、小鼠、猫、狗、兔子、狮子、牛、马、长颈鹿、老虎、江豚、黑白疣猴、环尾狐猴、雪貂,以及长寿的、高度抗癌的裸鼹鼠。
该研究的第一作者 Alex Cagan 博士描述道:“为了研究不同种类哺乳动物的体细胞突变,我们从寿命和体型各异的16个物种的56个个体中分离出208个单独的小肠隐窝,并对其进行了全基因组测序,以研究16种哺乳动物的体细胞突变景观。”
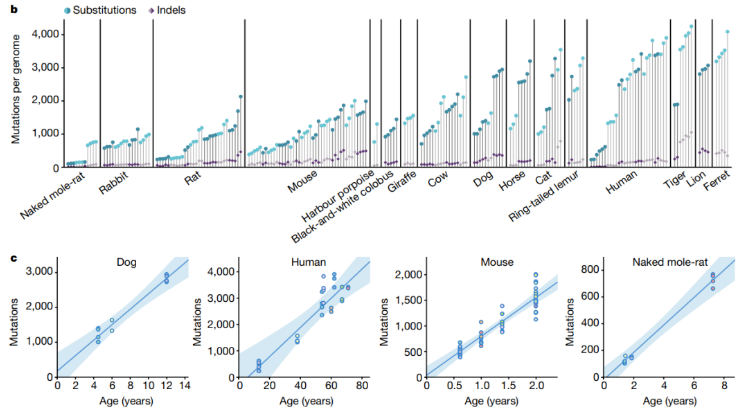
16种哺乳动物的体细胞突变发生率
值得注意的是,在体细胞突变中一个长期存在的问题是皮托悖论:在比较不同的物种时,患癌概率和体型之间没有明显关联。从理论上讲,体型较大的动物拥有更多的体细胞,那么它们发生体细胞突变的风险更大。然而,事实上在不同物种之间,体重和癌症风险之间似乎没有相关性。
对此,该研究的通讯作者 Inigo Martincorena 博士表示:“我们认为体型较大的动物进化出了更好的预防癌症的机制。但物种间癌症风险的进化降低是否部分是通过体细胞突变率的降低来实现仍然是未知的。如果体细胞突变有助于衰老,那么理论预测体细胞突变率可能与物种间寿命负相关。”
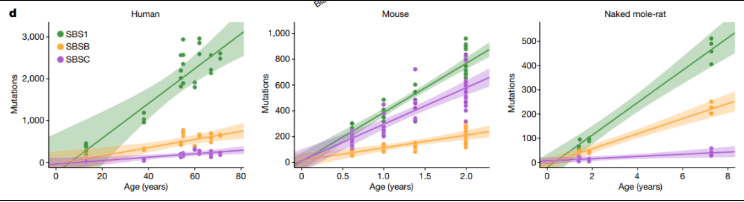
对人类、小鼠和裸鼹鼠样本的个体年龄的特征特异性突变负担的线性回归
通过全基因组对比分析,研究人员发现,在所有16个物种中,体细胞突变会随着时间线性累积。尽管被研究的16个物种在寿命和体重上存在巨大差异,但每个动物一生中获得的体细胞突变数量相对相似。平均而言,一头长颈鹿比一只小鼠大4万倍,而一个人的寿命是老鼠的30倍,但在寿命结束时,这三个物种的每个细胞的体细胞突变数量的差异仅为3倍左右。
这也印证了体细胞突变导致生物衰老的理论:每年的体细胞突变率在不同物种间差异很大,但均与物种寿命呈极强的负相关关系,这是一种其他生命史特征无法比拟的关联性。

体细胞基因突变率与物种寿命呈负相关
研究团队对皮托悖论的探索仍在继续。在比较寿命之后,研究人员发现体细胞突变率和物种体型之间没有显著的联系,这表明大型动物一定有其他机制去降低体细胞突变的风险。事实上,在自然界中,体型较大的动物往往拥有更长的寿命。
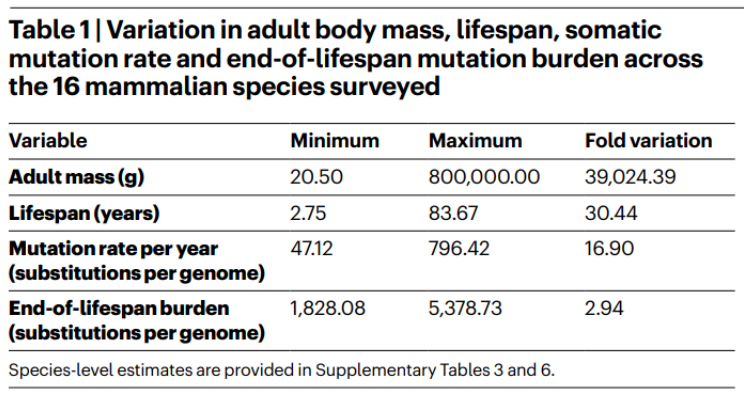
16种哺乳动物的成年体重、寿命、体细胞突变率和寿命末期突变负担的变化
衰老的确切原因仍然是一个尚未解决的问题,也是一个正在研究的热门领域。衰老很可能是由一生中细胞和组织的多种损伤累积引起的,包括体细胞突变、蛋白质聚集和表观遗传变化等。比较不同寿命的物种之间这些过程的发生率可以揭示它们在衰老中的作用,并指导长寿疗法的开发。
总的来说,这项研究提供了哺乳动物体细胞突变的详细描述,证实了物种寿命与体细胞基因突变率成反比,且与物种体型无明显关联。这些发现将有望改变我们对体细胞突变及其对进化、衰老和疾病影响的理解。
来自 生物世界